0-LeSAM: Adapt Segment Anything Model for Medical Lesion Segmentation
LeSAM:将 Segment Anything 模型应用于医学损伤分割

IEEE JOURNAL OF BIOMEDICAL AND HEALTH INFORMATICS, VOL. 28, NO. 10, OCTOBER 2024
背景
病变分割在医学图像分析中至关重要,但由于医学图像的复杂性和多样性,准确分割具有挑战性。现有深度学习算法受限于训练数据和模型特异性,难以通用。SAM 在自然图像分割表现出色,但直接用于医学图像分割时,因医学与自然图像领域差异,对不规则形状和低对比度病变分割效果不佳。已有研究尝试将 SAM 应用于医学图像,主要集中于器官分割,对病变分割关注较少,且依赖大量标注数据,未充分利用浅层特征。
- 提出 LeSAM,通过简单有效的策略将 SAM 适配于医学病变分割,提高其在不同成像模态下的病变分割性能。
- 开发特定于医学的图像编码器和任务特定的掩码解码器,融入医学领域知识,改善病变边界描绘。
- 通过全面实验验证方法在多种病变分割任务中的有效性和泛化能力。
实验方法
LeSAM 概述
LeSAM 保留 SAM 大部分结构,在原始图像编码器的每个变压器块中插入适配器模块,将提示编码器设为框模式,修改掩码解码器为 U 形结构。冻结原始图像编码器参数,使适配器模块、提示编码器和掩码解码器可训练。
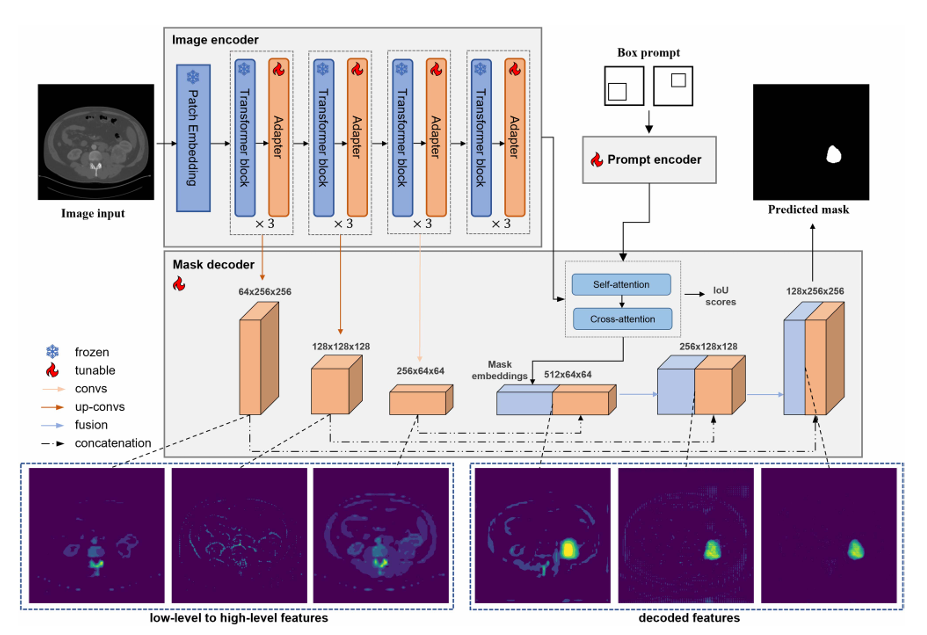
提出的 LeSAM 的架构。将适配器模块整合到每个 transformer 模块中,以集成特定任务的知识,并修改掩码解码器以改善与病变边界的对齐。原始图像编码器的参数被冻结,而适配器模块、提示编码器和掩码解码器被设置为可调。掩码解码器的中间特征图直观地显示在底部。
特定医学图像编码器
在原始图像编码器的每个变压器块中加入适配器模块,由下投影线性层、GeLU 激活和上投影线性层组成,引入医学特定知识,优化图像特征。(a)
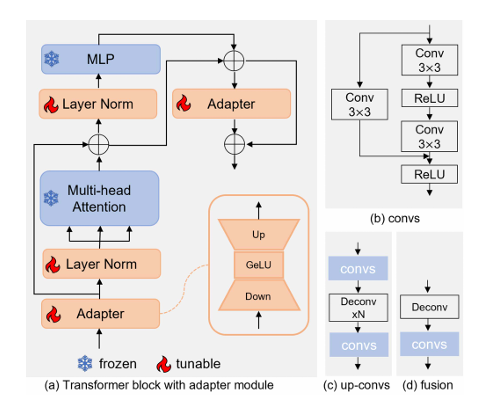
方法中采用的子块的架构。
任务特定掩码解码器
将掩码解码器设计为 U 形架构,利用卷积和上卷积操作处理不同分辨率的图像特征,通过融合和解码操作生成预测掩码,增强对不规则病变边界的描绘能力。(b)(c)(d)
渐进式训练策略
采用渐进式学习策略,先使用自监督预训练(MAE)结合无标签医学数据(RadImageNet)训练适配器模块,再用特定任务数据集训练适配器和其他可训练组件,使用 Dice 损失和交叉熵损失之和进行优化。
实验结果
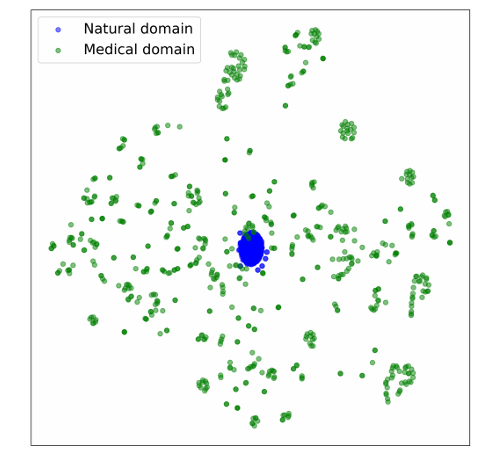
医学和自然的图像特征的流形。
在多个公共数据集上进行实验,涵盖不同模态和病变类型的医学图像。对图像强度值进行裁剪和归一化处理,将 3D 图像切片为 2D 图像,并生成框提示和随机扰动。
基于 Python、PyTorch 和 MONAI 库实现模型,使用 NVIDIA RTX 4090 GPU 训练。采用 AdamW 优化器和线性调度器,训练 50 个 epoch,初始学习率为 1e - 4。评估指标包括 DSC、IoU(用于 2D 图像)和 95HD、NSD(用于 3D 图像)。
分割性能
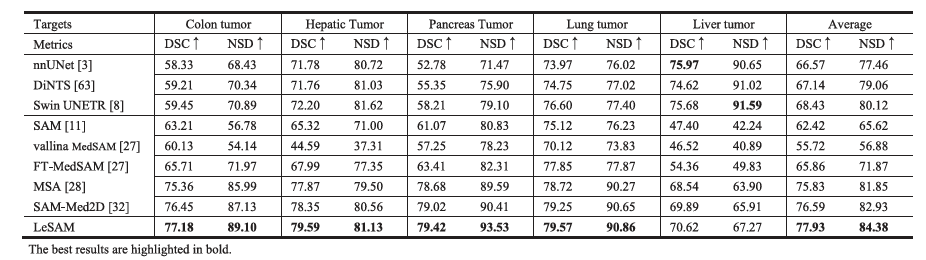
在 MSD 的五个 CT 肿瘤数据集上训练评估 LeSAM,与多种方法对比,LeSAM 在四个数据集上达到 SOTA,平均结果最优,能更好地描绘病变边界,但在肝肿瘤分割中仍有提升空间。
泛化能力评估
在不同模态和病变的数据集上评估 LeSAM 的泛化能力,与其他方法对比,LeSAM 在 7 个分割任务中的 4 个达到 SOTA,在其余 3 个任务中排名第二,证明其作为通用病变分割方法的有效性。
定性结果
通过可视化比较,LeSAM 在准确描绘肿瘤边界方面优于其他方法,有效缓解了过分割问题,改进了分割效果。
消融实验
适配器模块显著提高了 DSC 和 NSD 值;修改后的掩码解码器进一步提升了分割性能,尤其在 NSD 值上提升明显,可视化结果也证明其对肿瘤边界描绘的改进。
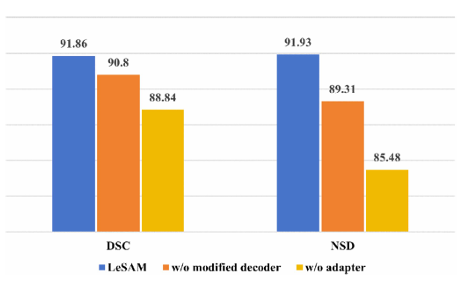
基于 KiTS19 的消融研究结果显示相应的平均 DSC 和 NSD 值。
总结
渐进式学习策略促进模型收敛;框提示的扰动会影响分割性能,大肿瘤相对更鲁棒,小肿瘤更敏感;模型在提示不足和低对比度病变情况下可能失败;LeSAM 性能依赖手动绘制框提示的准确性。
提出的 LeSAM 通过参数高效的适配技术和掩码解码器修改,显著提升了 SAM 在医学病变分割中的性能,在多种病变分割任务中取得优异结果,证明了适配 SAM 用于医学图像分割的临床意义。